
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
JCR | �p�d���OӋ�x��С����ˎ��ż�D�����^��Ч�����،��ί���
�����w�� �� �� С �� �r�g��2026��02��16�� ��Դ���Ї��ƌWԺ�Ϻ�ˎ���о���
�����]��
���� 2026��2��6�գ��Ї��ƌWԺ�Ϻ�ˎ���о������Q�n�}�M�c�Ї��ƌWԺ���������о����������F�������Journal of Controlled Release�ڿ��l�����}�顰Dual-payload small-molecule drug conjugates enable bystander anticancer activity with reduced nonspecific release�� ���о��ɹ��������Ե����һ�N�p�d��С����ˎ��ż�SMDC��Small Molecule-Drug Conjugate���OӋ����
2026��2��6�գ��Ї��ƌWԺ�Ϻ�ˎ���о������Q�n�}�M�c�Ї��ƌWԺ���������о����������F�������Journal of Controlled Release�ڿ��l�����}�顰Dual-payload small-molecule drug conjugates enable bystander anticancer activity with reduced nonspecific release�� ���о��ɹ��������Ե����һ�N�p�d��С����ˎ��ż�SMDC��Small Molecule-Drug Conjugate���OӋ���ԡ�
����һO�߰lչ������ˎ����A��ʽ��SMDC�{�������С���M���B�ԏ��ȃ��ݣ����[���ί��I���ܵ��V���Pע��Ȼ�������y���d��SMDC���R���������Դ����@�����ޣ��y�Լ��Ч�����c��ȫ�Կ��ơ���ǰ��ȫ��SMDC���P�о���Ҫ�۽��ڰ������w�������d�������չ�Լ��[���h��푑����B���ӵ��_�l��������������[������Ч����ͬ�r��Ч���Ͷ������á��،��ί����ڣ�����ԓ�I��ؽ��ͻ�Ƶĺ��ĿƌW���}�����о������Ե،��p�d�ɲ�������SMDC�wϵ���ڌ��F��Ч�[�������f�͵Ļ��A�ϳɹ��������^�߿��[��Ч�������@��������ˎ����خ��ԃ������l�Ķ����L�U���Ķ���SMDC�گ�Ч�c��ȫ��֮�g���Fϵ�y��ƽ���ṩ��һ�Nȫ�µ��OӋ��ʽ��
����Cԓ�OӋ���ԵĿ������c��Խ�ԣ��о��F���ǰ�������_�l�ĸΰ�����Ƕ���w��LIVTAC��Liver-Targeting Chimera����ģ���wϵ�������˵ڶ����p�d�ɷ���Bi-LIVTAC���w���о�������Bi-LIVTAC��ASGPR�߱��_�ĸΰ������У�չ�F�����چ��d��LIVTAC�ĵ�����Ч�ʺͿ��[�����ԡ��c��ͬ�r�������ڷ��ӳߴ������������|�ă�����Bi-LIVTAC��ASGPR�ͱ��_�����еı��Ӕzȡ���@�����ƣ����会�����ԳʬF�߶����w��ه�ԣ��ڶ�N��������ϵ�о�δ�^�쵽���@���ԣ��w�F�����õİ�ȫ�ԡ�������Ҫ���ǣ��о��F�ͨ�^�w����Bģ�ͣ��״����_�C���p�d��SMDC�ɮa���@�������^�߿��[��Ч���������w�ͱ��_�������[�����������^���Ŀ���ֳ���ã��߂�˷��[�����|�Եĝ�������Huh-7�ΰ���ֲ��ģ���У�Bi-LIVTAC��ˎ�ί����ɮa���@��������Ч�������cһ�����ΰ�ˎ�����������ã����Ɍ��F�[����ȫ���ˣ���δ���lѪС��p�ٵ��ڰж��ԣ�ϵ�y��ȫ�����á�ԓ�о����H�����C���p�d�ɲ�����ͬ������SMDC��Ч�c��ȫ�Է���Ī����ݣ������ڲ�ͬ�f�Ͱ��c�����~�����w����������d�ɣ��缚�����غ͟ɹ�̽ᘣ��wϵ�о��@���˳ɹ���C���w�F��ԓ���ԵďV���m�����cƽ�_��������
�Ϻ�ˎ�����c�Ї�ˎ�ƴ�W�ʿ�о���ꐴ��ܡ�������������ʿ�о��������q�����ˎ�ƴ�W��Tʿ�о������Ȟ鱾Փ�ĵĹ�ͬ��һ���ߣ��Ϻ�ˎ�������Q�о��T�������������������о��T��Փ�ĵĹ�ͬͨӍ���ߡ�ԓ�����õ��ˇ��ҿƼ��ش�헡�������Ȼ�ƌW���������Ŀ���Ї��ƌWԺ�˲�Ӌ�����Ŀ���Y����
ȫ��朽ӣ�https://doi.org/10.1016/j.jconrel.2026.114695
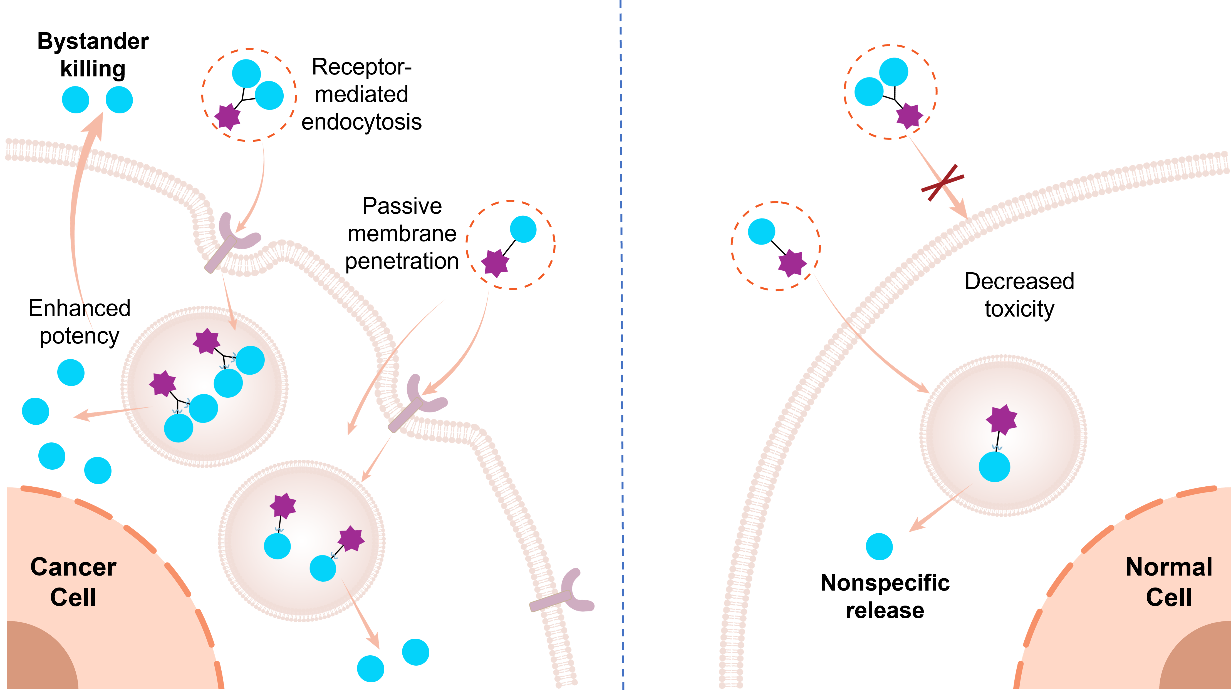
�p���dSMDC�OӋ����ʾ��D
�����岿�T�����Q�n�}�M��