
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
[�W�g���] �����ƌW�WԺ���ڶ����وF�ʾKLF6��Ѫ��������ʧ���T��Ѫ�܃�Ƥ�����F�������P�I�D�����
�����w�� �� �� С �� �r�g��2026��02��19�� ��Դ���Ї��ƌWԺ��W�����ƌW�WԺ
�����]��
���� ���գ��Ї��ƌWԺ��W�����ƌW�WԺ���ڶ������n�}�M�����һ��P�ڄ��}����Ӳ���l���C�Ƶ�ͻ�����о�����ʾ���D�����KLF6��Ѫ�܃�Ƥ������������Ѫ���������еĺ��ı��o����
���գ��Ї��ƌWԺ��W�����ƌW�WԺ���ڶ������n�}�M�����һ��P�ڄ��}����Ӳ���l���C�Ƶ�ͻ�����о�����ʾ���D�����KLF6��Ѫ�܃�Ƥ������������Ѫ���������еĺ��ı��o���á�ԓ�о����ö��Ƶ������b��ģ�M�w��Ѫ���h�� (�D1)���C���˟oՓ���^��߀���^�͵ļ���������ͨ�^����KLF6���_�����l��Ƥ�����l�����F��������Ferroptosis�����Ķ���ʾ�˄��}�߉K�ðl��Ѫ�ֲܷ�̎���������W���әC�ơ�
KLF6�Ǹ�֪Ѫ�������ġ��ڱ�����Ѫ�܃�Ƥ�����r�̳�����ѪҺ���Ӯa���ļ����������������ȵČ�����������Ѫ�ܾ��б��o���ã������}�ֲ桢����̎��Ҋ�ĵͼ���������ʎ�������t�DŽ��}����Ӳ����AS���ĸ�Σ���ء����о�ͨ�^�����w������ϵ�y������Ѫ�܃�Ƥ����ʩ�Ӹߡ��ͼ������������̼�������������ǣ��о��l�F���H�ͼ�������LSS�����^��������HSS��ͬ�ӕ�����Ƥ�����p�����@�ɷN�����������������@�������˼�����KLF6�ı��_ˮƽ���������˼���������ͨ�^ʹ���F�����خ������Ƅ���Fer-1���M�и��A���C���@�N�ɮ����������T�����F�����ǿ���� (�D2)��
ͨ�^RNA�y������ķ�������W��C���о��F�����KLF6�{���F�����ľ��w�pͨ·�{���F�����ķ��әC�� (�D3)��һ��BiP-PERK-SLC7A11ͨ·��KLF6���_���{�����ƃ��|�W�����{�����ף�BiP, PERK�����װ����D�\�wSLC7A11�ı��_��������������������������MVD-ID11-CoQ10ͨ·��KLF6߀ͨ�^�{�ؼ��u����;����MVD���Ͷ���������Ó��ø��IDH11����Ӱ��oøQ10��CoQ10���ĺϳɣ��M���{��֬�|�^����ˮƽ���о��@ʾ���ڵͼ������������l���£����|�W������̖ͨ·�������ƣ����^���_KLF6�܉�֏��@Щ���ı��_������C11 BODIPY����ˮƽ���Ķ������F������
����ģ�M���ӽ��w�ȵIJ����h�����о��ˆT߀�����˰���Ѫ��ƽ���������͆κ˼����Ĺ����Bģ�͡��Y���������ڵͼ������l���£��^���_KLF6���H�ܜp�ك�Ƥ������֬�|�^������߀���@�����͆κ˼�����𤸽�Լ�֬�|��Ѫ�ܱڵķe�� (�D4)��ԓ�о��״�ϵ�y�Ե��C����KLF6���B��Ѫ�������W�����c��Ƥ�����F�������P�I���ӹ��c���@һ�ɹ����H����˞��Ѫ�ֲܷ�̎��Ѫ���Ɂy�^�����װl�����}����Ӳ��������ͨ�^����KLF6���F����ͨ·���������XѪ�ܼ����ṩ��ȫ�µ���Փ�����͝����ί����c��
�����о��ɹ���2025��10��31����Abnormal shear stress induces
ferroptosis in endothelial cells via KLF6 downregulation�����}����ʽ��eLife�ڿ���䛡�ԭ���B�ӣ�https://doi.org/10.7554/eLife.109140.1.sa2
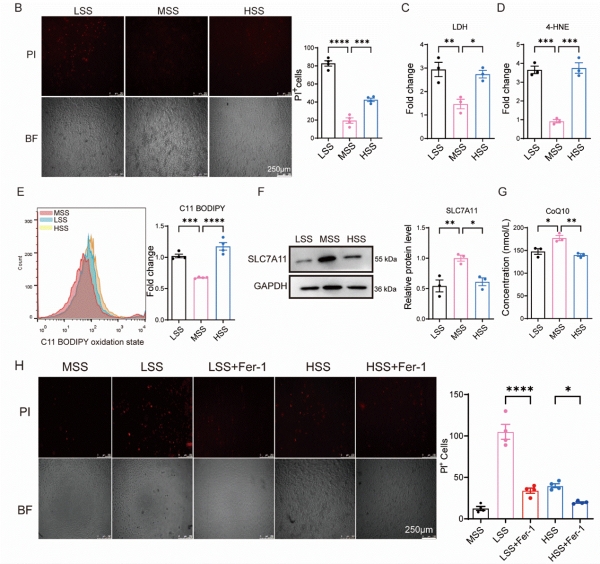 �D2 �������Б�������Ѫ�܃�Ƥ�����F����
�D2 �������Б�������Ѫ�܃�Ƥ�����F����
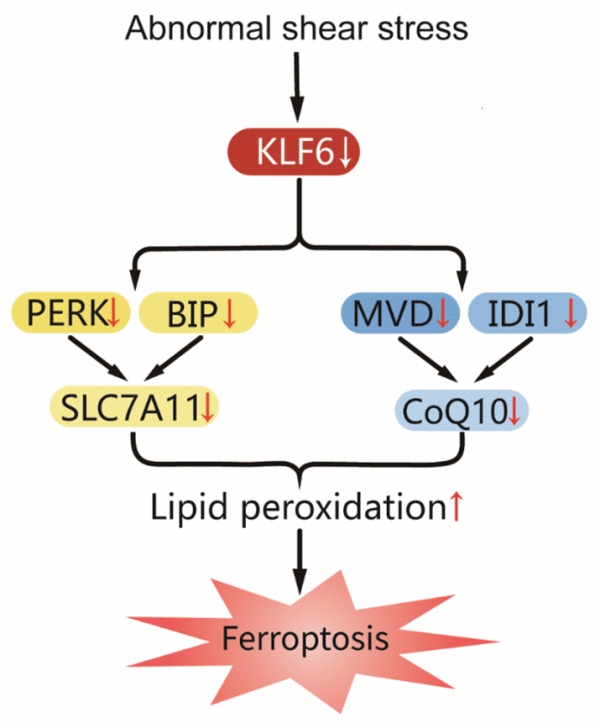 �D3 �������Б���������Ƥ�����F�����ķ��әC��
�D3 �������Б���������Ƥ�����F�����ķ��әC��