- ��� ���ՄӑB(t��i) �˲��Ј� �¼��g(sh��)���� �Ї��ƌW(xu��)�� ��չ�_ ���v��ֱ�� ��չ���� �r���� ���g(sh��)��Ӎ ���Mԇ��

-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
Nature Communications | �����䡢�������ʽ��A�F�����ʾ�M����H3K4me1��������ֲ���еĹ���
�����w�� �� �� С �� �r�g��2026��02��20�� ��Դ����(f��)����W(xu��)�����ƌW(xu��)�W(xu��)Ժ
�����]��
����2026 �� 2 �� 16 �գ���(f��)����W(xu��)�����ƌW(xu��)�W(xu��)Ժ����������n�}�M�����������о��T�n�}�M�c�ʽ��A�о��T�n�}�M�������ڡ���ȻͨӍ���� Nature Communications ���ھ��l(f��)�����}�顰 H3K4me1 directs H3K36me2 and H3K36me3 deposition in land plants �� ���о�Փ��
2026��2��16�գ���(f��)����W(xu��)�����ƌW(xu��)�W(xu��)Ժ����������n�}�M�����������о��T�n�}�M�c�ʽ��A�о��T�n�}�M�������ڡ���ȻͨӍ����Nature Communications���ھ��l(f��)�����}�顰H3K4me1 directs H3K36me2 and H3K36me3 deposition in land plants�����о�Փ�ġ�ԓ�о��״ν�ʾ��H3K4me1��������ֲ���еĪ��ع��ܣ�H3K4me1�ɱ��ض���x�������R�e���M����ļH3K36���D(zhu��n)��ø�����MH3K36me2��H3K36me3��Ľ�����
�M�����g�����post-translational modifications, PTMs�����D(zhu��n)��{(di��o)���аl(f��)�]�P(gu��n)�I���ã����V�����c����������L�l(f��)�����h(hu��n)��푑�(y��ng)�ȶ�N����W(xu��)�^�̡�PTMs���ض��ġ����롱ø�͡�������ø�ӑB(t��i)�{(di��o)�أ����ɱ���ͬ�ġ���x���������R�e�����У��M����H3��4λه���ᣨH3K4���������о������������֮һ���䲻ͬ���B(t��i)���μ����������������������ɷքe��(bi��o)ӛ�D(zhu��n)䛼�������ơ���������У�H3K4�μ�����H3K4me1������ѱ��C���������ӵĘ�(bi��o)ӛ��Ȼ������ֲ���еĹ����в����_��
���������ƌW(xu��)���}���xȡ�ˆμ�(x��)��ˮ�����R�����塢���ڵ����С�����\�Լ��_��ֲ��M�Ͻ��ˮ�����M�б��^����M�������l(f��)�F(xi��n)���ֲ����H3K4me1��ȫ����M������(n��i)�ķֲ�ģʽ�����c�����D(zhu��n)䛵����P(gu��n)�Ծ��ʬF(xi��n)�����ص���������ʾH3K4me1�����ֲ���п��ܾ��в�ͬ����������Ĺ��ܣ��Da�����������ʾH3K4me1�����ֲ���еĹ��ܣ��Y�x���خ����R�eH3K4me1����x����Ehd3��Early heading date 3�������w�Y(ji��)��(g��u)����������Ehd3ͨ�^�䴮(li��n)PHD�Y(ji��)��(g��u)��tandem PHD finger domain���خ��R�eH3K4me1���ԓ�R�eģʽ�c��֪��PHD�Y(ji��)��(g��u)����ȫ��ͬ���Db�������ܻ؏�(f��)����@ʾ��ͻ׃Ehd3���R�eH3K4me1���P(gu��n)�I������o�����ehd3-1ͻ׃�w���������ͣ��f��Ehd3��H3K4me1���R�e����l(f��)�]����W(xu��)���������衣�Mһ��ͨ�^IP-MS�ȼ��g(sh��)���b����Ehd3�ĽY(ji��)�ϵ���H3K36���D(zhu��n)��øSDG724��SET domain group 724�����Dc���������c�M�W(xu��)�����l(f��)�F(xi��n)��Ehd3��SDG724ȱʧ����(d��o)��ֲ�������L�l(f��)�����D(zhu��n)䛽M�����^����M������F(xi��n)�����Ƶ�׃��������Ehd3��SDG724�ͽM�������ChIP-seq�Y(ji��)�����l(f��)�F(xi��n)Ehd3��SDG724�cH3K4me1�����ȫ����M��������λ����ehd3-1��sdg724-1��ehd3 sdg724ͻ׃�w�У�H3K36me2/me3��ȫ����M�ֲ��l(f��)��һ���Ե�ȫ�ָ�׃���Dd�����w��ø���Mһ���C����SDG724��H3K36���D(zhu��n)��ø������ه��Ehd3��H3K4me1�Ĵ��ڣ��De���������N�M�W(xu��)�����@ʾ�������ֲ����H3K4me1�cH3K36me2/me3��ȫ����Mˮƽ�Ͼ����@���Ĺ���λ�������C�����������о�ϵ�y(t��ng)�U����H3K4me1�����ֲ���н錧(d��o)H3K36me2/me3�����ķ��әC�ƣ���ʾ��H3K4me1��ֲ���о����c��������ȫ��ͬ�Ĺ��ܡ�
�B�d��W(xu��)�����c�h(hu��n)���ƌW(xu��)�W(xu��)Ժ�v���Ǽѱ�����(f��)����W(xu��)��������ڈF꠲�ʿ�о�������衡��Ĵ��r(n��ng)�I(y��)��W(xu��)ˮ���о��������ڶſ����Լ�̩�W(xu��)Ժˎ�W(xu��)Ժ�v����fƽ�鱾�Ĺ�ͬ��һ���ߡ���(f��)����W(xu��)�����ƌW(xu��)�W(xu��)Ժ��������ڡ����������о��T���ʽ��A�о��T�鹲ͬͨӍ���ߡ���(f��)����W(xu��)�����t(y��)�W(xu��)�о�Ժ�{(l��n)쳌���Ҍ��������ṩ����Ҫ֧�֡��Ї��ƌW(xu��)Ժ�Ϻ��ߵ��о�Ժ�Ϻ���Դ��SSRF���ƌW(xu��)���ġ����ҵ����|(zh��)�ƌW(xu��)�о����Ϻ����O(sh��)ʩҎ(gu��)ģ�������|(zh��)�Ƃ�ϵ�y(t��ng)�鱾�о��ṩ�˼��g(sh��)֧�֡����о��õ��ˇ������c�аl(f��)Ӌ����������Ȼ�ƌW(xu��)�����������������YԴ�l(f��)���c���Ç������c������_���n�}�Ŀ���Y����
ȫ���B�ӣ�https://doi.org/10.1038/s41467-026-69632-5
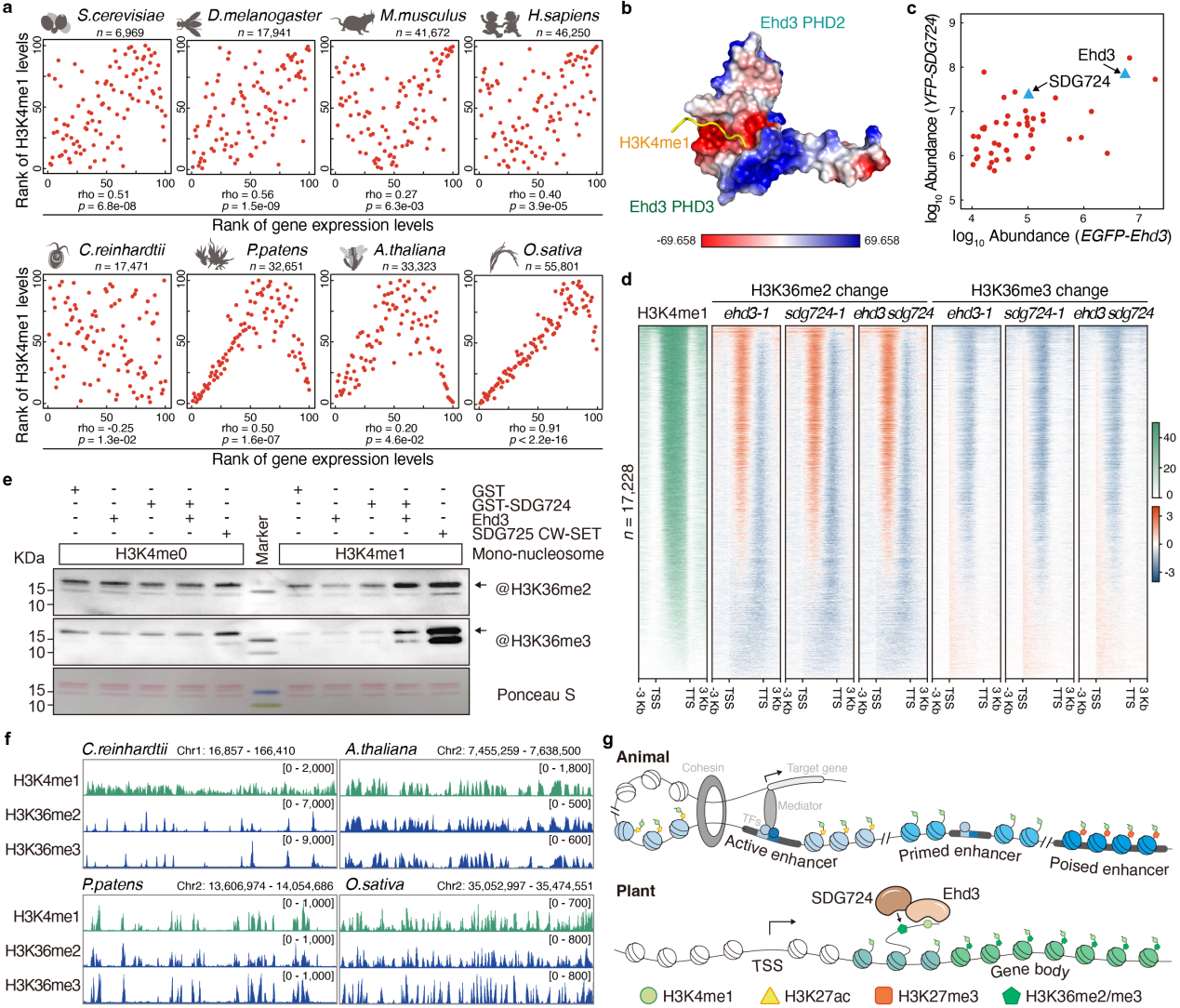
a.���ֲ����H3K4me1�c������_�ʬF(xi��n)�����ص����P(gu��n)�ԣ� b. Ehd3��(li��n)PHD�Y(ji��)��(g��u)���R�eH3K4me1�Ķεľ��w�Y(ji��)��(g��u)��c. Ehd3�cH3K36���D(zhu��n)��øSDG724��������ã� d.Ehd3��SDG724ȱʧ��(d��o)��H3K36me2/me3�ķֲ�ģʽ�l(f��)��ȫ��׃���� e.ø���C��SDG724�ļ��D(zhu��n)��ø������ه��Ehd3��H3K4me1�� f. ���ֲ����H3K4me1�cH3K36me2/me3����λ�� g. H3K4me1�ڄӡ�ֲ���о��в�ͬ�Ĺ��ܡ�
 ����ͨ�Ź���̖
����ͨ�Ź���̖
���ѣ�
֪����I(y��)��Ƹ
���ՄӑB(t��i) | �˲��Ј� | �¼��g(sh��)���� | �Ї��ƌW(xu��)�� | ��չ�_ | BioHot | ���v��ֱ�� | ��չ���� | �r���� | ���g(sh��)��Ӎ | ���Mԇ��
���(qu��n)���� ����ͨ
Copyright© eBiotrade.com, All Rights Reserved
(li��n)ϵ���䣺
��ICP��09063491̖