
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
�����WԺꐇ����Fꠘ������}�m�������}�����ľ��N�����F�_�Űl�ͺϳ�PHA
�����w�� �� �� С �� �r�g��2026��02��25�� ��Դ�����A�@�����WԺ
�����]��
�������ľ��N����������a�I�ġ�оƬ�����Q���˰l��ˇ��Ч�ʡ��ɱ��c�aƷ����������ǰ���҇���������a�I�ĺ��ľ��N��80%��ه�M�ڣ��Ĵ��ڰ����ᡢ�ЙC�ᵽø�Ƅ����T���P�I���a������ه���⡣�@һ���治�H�Ƹ��˼��g���M�c��ˇ�m��ijɱ������ڮa�I朹���朌��������[���������{����������ґ��ԡ������I���������M�ı����£�����������N�������ɿ��ѳɞ���ͻ�Ƶđ���ƿ�i��ꐇ������ڈF꠲ŏ�Ұ���h���з��x�õ����}�A...
���ľ��N����������a�I�ġ�оƬ�����Q���˰l��ˇ��Ч�ʡ��ɱ��c�aƷ����������ǰ���҇���������a�I�ĺ��ľ��N��80%��ه�M�ڣ��Ĵ��ڰ����ᡢ�ЙC�ᵽø�Ƅ����T���P�I���a������ه���⡣�@һ���治�H�Ƹ��˼��g���M�c��ˇ�m��ijɱ������ڮa�I朹���朌��������[���������{����������ґ��ԡ������I���������M�ı����£�����������N�������ɿ��ѳɞ���ͻ�Ƶđ���ƿ�i��
ꐇ������ڈF꠲ŏ�Ұ���h���з��x�õ����}�A�����}����Halomonas spp.����Ȼ���꣬�_չ�˶�ʮ������ϵ�y���P���ɹ����Ƴ�������ȫ����֪�R�a������͵ױP��������Halomonas bluephagenesis TDϵ�м����������꣬���F���_�ŗl�����B�m�l�ͣ��ص�Ҏ�ܜ���h�����@�������ܺ��c�O��ɱ����ڇ��H���״�����������˻��ژO���������һ�����I���\�g��NGIB����Ȼ�������}���ױP��ه�^���}�ȣ�ͨ��30-60 g/L NaCl���ԾS�ּ����������B�c���x���ԡ��@һ���}��ه��һ���̶������������ڸ����}�����`�ˇ�wϵ�еđ�����չ��Ҳ�����˺��m�Uˮ̎���c�h��ؓ�ɡ�����ڱ����_�ŷǟo�����B���ݵ�ͬ�r���������}�������}�h������ه���Ķ����������ܡ�����̼�������m�ć��a������������ƽ�_����ԓ�I��ؽ��ͻ�Ƶĺ��ĿƌW���}��
ᘌ���������ꐇ����n�}�M���õ������̻�������ԣ�ϵ�y��������ĵ��}�m���ԣ��ɹ��������ڃH��0.1%��w/v��NaCl�l�����Կɷ������L��SSMϵ�й��̾��ꡣ���о����@ԓϵ�о���Ę���߉�����}�m���C�Ƽ�������ϳ�����չ�_ϵ�y�U���������}���ױP�ľ��������̸����ṩ�·�ʽ��Ҳ���҇�����֪�R�a��I�������ȃ����c�a�I�����õ춨��Փ�����c���g���䡣
2026��2��11�գ����A��W�����ƌW�WԺꐇ����n�}�M�ڡ����\�gڅ�ݡ���Trends in Biotechnology�����ھ��l�����}�顰���̻������}�ΰ������F���}�l���µ��_��ʽ�ǟo�����u������ϳɡ���Engineering Halomonas for Low Salt Open Unsterile Production of Polyhydroxybutyrate�����о�Փ�ġ�ԓ�о������}��Halomonas bluephagenesis���о�����ͨ�^ϵ�y�ԵĹ��̻����죬������һϵ���ڵ��}�l�����Ա��ַ������L�����Ĺ��̻����ꡣ���õ���ʽ�������x�����Ĺ��̲��ԣ�����݆�Y�x�c�����Ы@���˸߶��m�����}�h����H. bluephagenesis TD1.0 SSMϵ�о��ꡣԓϵ�о������}����̓H0.1%��w/v��NaCl��pH = 9�ĸ߉A�ԗl�����Կɷ������L��ͬ�r�������ڸ��}�h���е��������ԣ��Ķ��@����չ�����}���ĝB���m�����������о������}���ױP�ľ��������̸����ṩ�·�ʽ��Ҳ���҇�����֪�R�a��I�������ȃ����c�a�I�����õ춨��Փ�����c���g���䡣
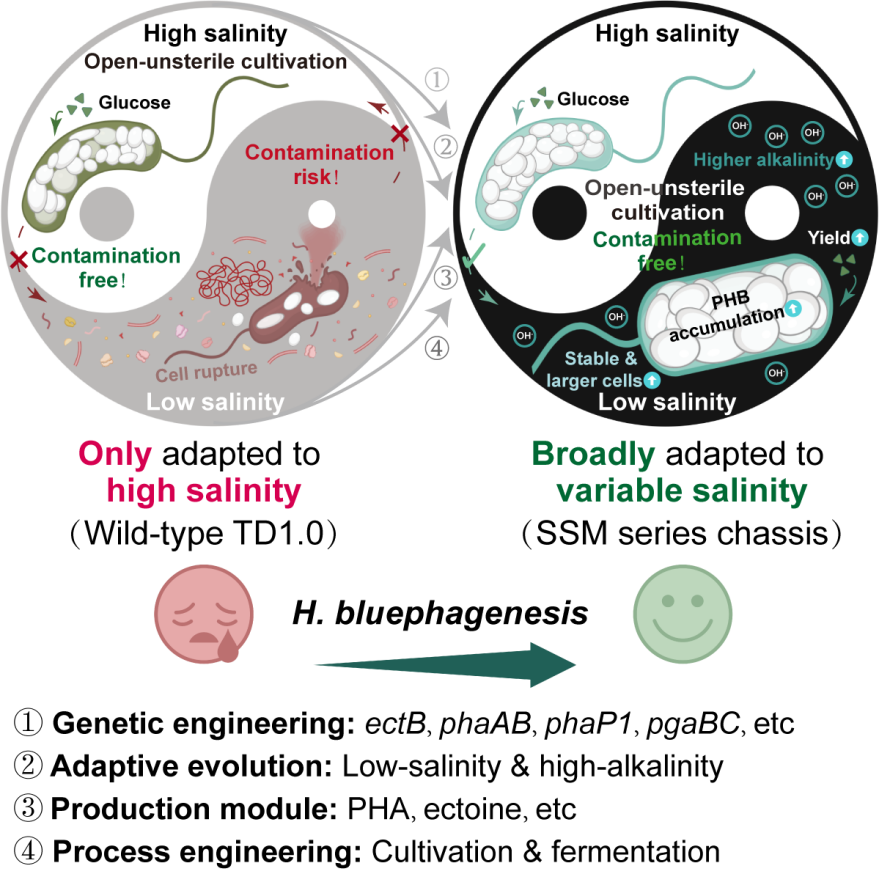
�D1. �D��ժҪ
�о��FC���\���˻������m���Ԍ�����M�������x�ؘ��Լ��l���^�̹��̵ȶ�N���ԣ���H. bluephagenesis�ĝB���{�ء������ΑB�c���x�W�j�M����ϵ�y��������M�W�c���ͷ����Y���@ʾ�����}�m���;����ڼ����������|�������ΑB��Ⱥ�w�О�ȷ���l�����@����׃�����F�鼚���w�e�����l���������Լ�����ϳ����������w��������7 L���ﷴ�����У�ԓ���̾����ڃH����5 g/L NaCl�ĵV�����B���l�͗l���¼��Ɍ��F�������_�ŷǟo�����B������44С�r�ȫ@����s 76 g/L �ļ������أ����� PHB �������_ 86%��̼Դ���������ǵ�PHB���D���ʼs 39%�������Y��������ԓ���̻����}���wϵ���@�������}����ه��ͬ�r���Կɱ��փ����ҷ����������������ܣ����H��δ�����ܡ���̼���ͳɱ��Ĺ��I���\�g·���ṩ�˿��з�ʽ��Ҳ��չ�����}���ڸ��V����ˇ�l���µđ��Ý��������⣬���о�ϵ�y��ʾ�����}���ڵ͝B�h���µ��m�����ؘ���������������������B���m���c�h��푑��C���ṩ����Ҫ�����A���µ��о��C����
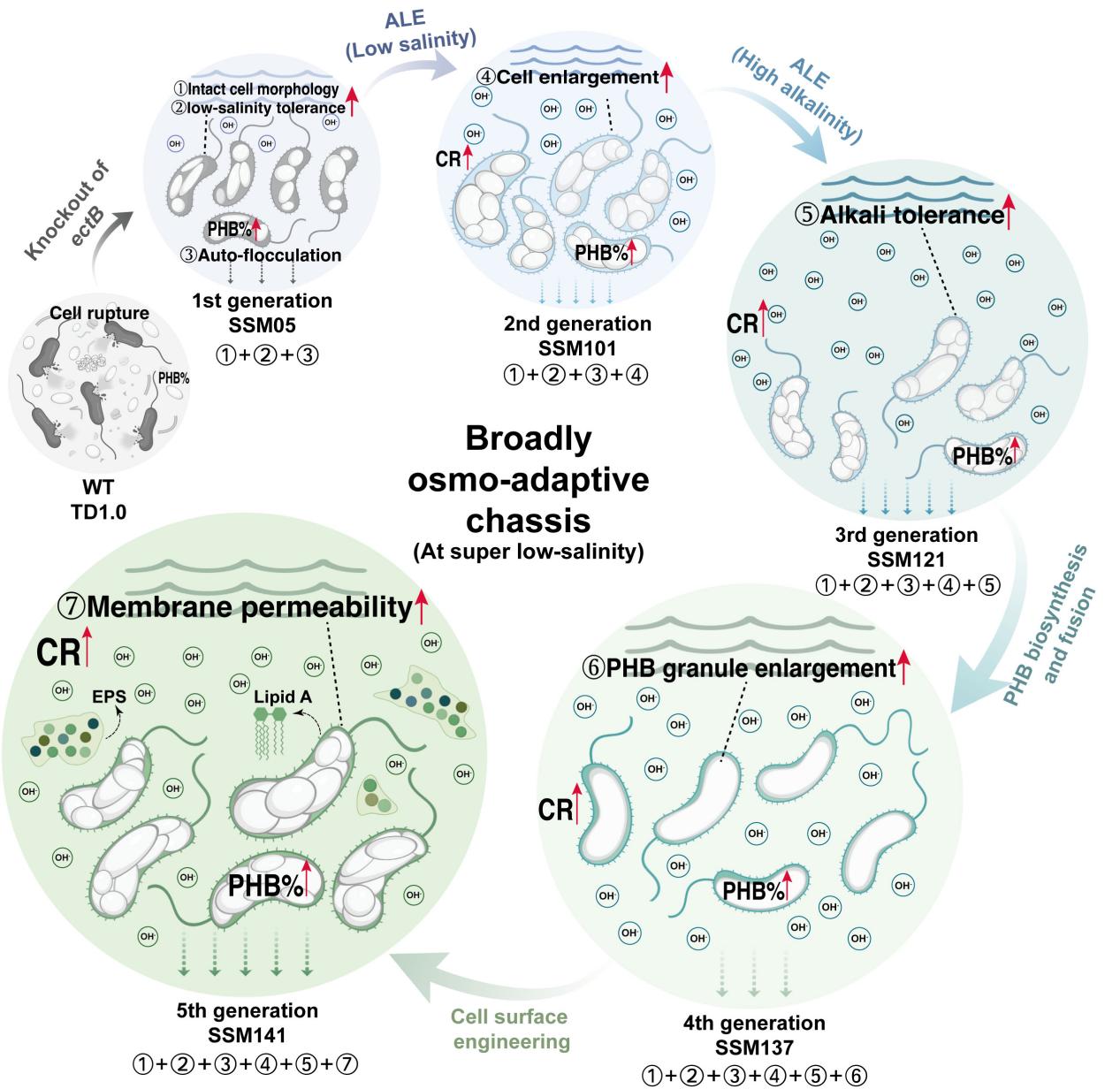
�D2. �������̻����옋���ďV���}���m����H. bluephagenesis SSMϵ�еױP��ģʽ�D
���A��W�����ƌW�WԺꐇ������ڞ鱾��ͨӍ���ߡ�2021����ʿ�о����O˼��鱾�ĵ�һ���ߣ�2022����ʿ�о�����������2024�ò�ʿ���I����������2025�ò�ʿ���I�����Ʒ���2024�ò�ʿ���I������骞鱾�о�������Ҫؕ�I���Ǹ��帱�о��T���c���n�}ָ���c���������о��õ��Ƽ����������c�аlӋ���͇�����Ȼ�ƌW������Y����ͬ�r�@�ñ��������S�����A�����������ƌW�����Լ����A��W�����t�W������������Rƽ�_�Ĵ���֧�֡�
ԭ��朽�
https://doi.org/10.1016/j.tibtech.2026.01.002