
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
Cell Stem Cellح�Ї��ƴ����t�����ĈF�ʾ�c����Ƥ�ޏ͵ġ��z���c���C��
�����w�� �� �� С �� �r�g��2026��02��25�� ��Դ���Ї��ƌW���g��W | �����ƌW�c�t�W��
�����]��
���� 2026 �� 2 �� 23 �գ��Ї��ƌW���g��W�����ƌW�c�t�W�������ߑ����c�����ί�ȫ�����c����� ���� ���ڈF��� Cell Stem Cell �l��Փ�ġ� VIPR1 acts as an enteric neural checkpoint that suppresses intestinal stem cell-driven epithelial regeneration and exacerbates colitis �� �� �״�����{���c����Ƥ�ޏ������ġ��z���c���C��
�S�����I���M�̼ӿ죬IBD�ѳɞ��ش����Լ������M�ܿ�TNF����IL-12/23p40�������Ƅ���Ч�����װY����ԭ�l��푑����^�lʧЧ�ߏͰl�������R���y�}��Խ��Խ���C�������������Q���L���A��IJ��džμ��װY���ƣ������Ĥ�ǷF��Ч���ϣ�����Ƥ�ޏ��Ǻ��ĭh����Ȼ�������װY�h���У���Ƥ�ޏͳ����������ƣ�����әC�ƺͿɸ��A���c�Բ�������
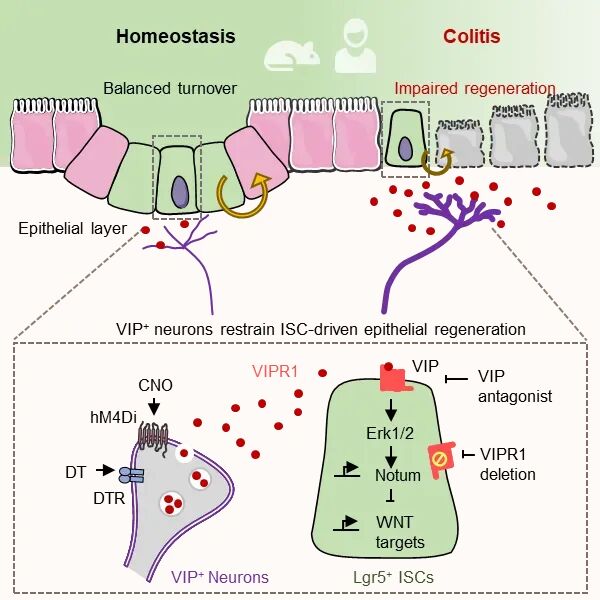
2026��2��23�գ��Ї��ƌW���g��W�����ƌW�c�t�W�������ߑ����c�����ί�ȫ�����c������������ڈF���Cell Stem Cell�l��Փ�ġ�VIPR1 acts as an enteric neural checkpoint that suppresses intestinal stem cell-driven epithelial regeneration and exacerbates colitis�����״�����{���c����Ƥ�ޏ������ġ��z���c���C�ơ��о���ʾ�����װY���c�� (IBD) �������װY�У�VIP����Ԫͨ�^ֱ�Ӽ���ɼ������wVIPR1��������Ƥ���������Ӿ��Ĥ���ϲ������װY�Mչ���_������ϵ�y���c����Ƥ�ޏ͵��P�I�T�����á�

��ǰ���F���2024��6����Cell Host & Microbe������c�����P�c����a�����Ұ���tyramine���ɼ���ɼ���������2A�I�����������w��������Ƥ�ޏ͡��Ӿ��Ĥ���ϲ������װY��������2A���w�x��������Yohimbine������@һ����Ч�����@�����M��Ƥ�ޏͲ������c�ף��w�F�ˡ���ˎ���á��ĝ����D���rֵ��ԔҊBioArt����������c�uCell Host Microbe | ����/���/���ꖰl�F�c��������c���ɼ�����ֳ�����c�ęC�Ƽ����A��������
�ڴ˻��A�ϣ����о��Mһ���۽���Դ��̖���c����Ƥ�����ϵ�y��̖���R�Ľ���M�������m�����������{�أ�������̖�Ƿ���Ƥ�ޏ��������P�I�{�����ؼ������c�דp���ޏ��еęC�ƣ��L��δ�����F����������ƽ�_�Ͷ�N�w���z���{���ֶΣ�ϵ�y������VIP����Ԫ���װY��������Ƥ�������������á��Y��������VIP��̖ͨ�^VIPR1-ERK-Notum�S�{�ظɼ���WNTͨ·�������{���װY����Ƥ�p���c�ޏ�ģʽ�����r�g�c��������ӛ�������L���װY�^������Ƥ�ޏ͵ĄӑB܉�E�����ػ�����A����Mһ���C�������ԓ�������S���@���֏���Ƥ�ޏ������������Ĥ���ϲ������c�ױ��͡�
ԓ�о�ϵ�y��ʾ����ϵ�y����Ƥ�ޏ͵��������{�ؙC�ƣ��������Ĥ�����ʡ��_�l���ʹ��ޏ��A�����ṩ�����_����Փ���A�͝����D������
�Ї��ƴ����Ľ��ڞ����µ�ͨӍ���ߣ���ʿ������Ͳ�ʿ�����úÞ鱾�����Ĺ�ͬ��һ���ߡ��@������Ҳ�@�ö�λ�����ߵĴ����������Ї��ƴٵ�һ�tԺ�����Ə��_�������ṩ��IBD���˽M���ӱ����Ї��ƴ�������ں��ܘs�����Ҳ�ṩ�ˌ��֧�ֺ�ָ����Ҋ��
ԭ��朽ӣ�https://www.cell.com/cell-stem-cell/abstract/S1934-5909(26)00032-9