
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
���وF��_�l���w�S�����ٺͼ����fͬ�����mRNA-LNPϵ�y���ڿ˷��η��w�S���ί��е��f������
�����w�� �� �� С �� �r�g��2026��02��28�� ��Դ��������Wˎ�WԺ
�����]��
���� ���Q�������𣬱�����Wˎ�WԺ��Ȼˎ�P����ˎ��ȫ�����c����������о��T�F���2026��2��23���� Journal of the American Chemical Society �ھ��l�����}�顰FAP-Synergistic Organ-Targeted mRNA-LNP for Overcoming Delivery Barriers in Hepatic and Pulmonary Fibrosis�����о�Փ��
�w�S��������һ��Լ�������|�^�ȳ��e����Ҫ�����IJ����^�̣������¸Ρ��ε����ٹ����ܓp��Ŀǰ�R���ί��ֶ����ޣ���Ч�в����롣mRNA�����ڻ����ί��I��չ�F���V�ǰ��������Ό����Ч�f�����w�S�������еİм��������ij��w�S��������ͻ�����ܵļ�������|���ϲ����F�����خ��Ԕzȡ�����Ǯ�ǰ���R���P�I����
֬�|�{���w����ĿǰmRNA�f�͵������d�w��������еĸΰ������������ڸ����w�S��������w�S�����еđ��á��������ͨ�^�{��LNPs�M�ֿ���һ���̶��ό��F�����x�����f�ͣ����w�S���M���еĮ���ECM�ԕ���K�{�����B�����⣬�ο��������w��������y��ͬ�r�M�������x�����c�����خ��Ե��p��������ˣ�ؽ��lչ������ٰ����c�����R�e�����ľ����f��ϵ�y��

���Q�������𣬱�����Wˎ�WԺ��Ȼˎ�P����ˎ��ȫ�����c����������о��T�F���2026��2��23����Journal of the American Chemical Society�ھ��l�����}�顰FAP-Synergistic Organ-Targeted mRNA-LNP for Overcoming Delivery Barriers in Hepatic and Pulmonary Fibrosis�����о�Փ�ġ��о��F�����ͨ�^Ugi���M�ַ��������˿���x��x��֬�|�죬���Y�x�����иλ���x�����f��������LNPs���Mһ���������w�S���^���خ��Ը߱��_�ij��w�S��������ף�Fibroblast activation protein, FAP����С�������w���OӋ���ϳ��˃ɷN����֬�|��N-FL��G-FL��������������LNPs�У��������w�S�����ٺͼ����fͬ�����f��ƽ�_��fibrosis organ and cell uniffed-targeting system, FOCUS�������F��mRNAˎ���ڸ��w�S���ͷ��w�S���M���Ќ�������ij��w�S�����ľ����f�ͣ����w�S���������ί��ṩ���µ��f�Ͳ��ԡ�
�w�⌍��C����FOCUS LNPs��FAP�^���_��HT1080�������DȾЧ�������s5�����ڲ���ù���T���ķ��w�S��С���CCl4�T���ĸ��w�S��С��ģ���У�FOCUS LNPs�ڳ��w�S�����еķֲ��@�����ӣ��w�S���^��ȵğɹ���ø���ױ��_ˮƽҲ�õ����@������ؓ�dPentraxin-2 mRNA��mPTX-2����FOCUS LNPs�ڃɷN�����w�S��ģ��С���о����F���@���Ŀ��w�S��Ч�������w�S��ģ�����zԭ���e�p�ټs80%�����w�S��ģ���Мp�ټs70%���ү�Ч�����ؽMPentraxin-2���ס��C���о��@ʾ��mPTX-2 FOCUS LNPsͨ�^���Ɔκ˼������w�S�����ֻ����p��M2�;��ɼ����O���Լ����Ƴ��w�S��������l�]����c���w�S�����á���ȫ���u���Y��������FOCUS LNPsδ�������@ȫ�����ԣ��Ҳ�Ӱ������������ϣ�������������õİ�ȫ�ԡ�
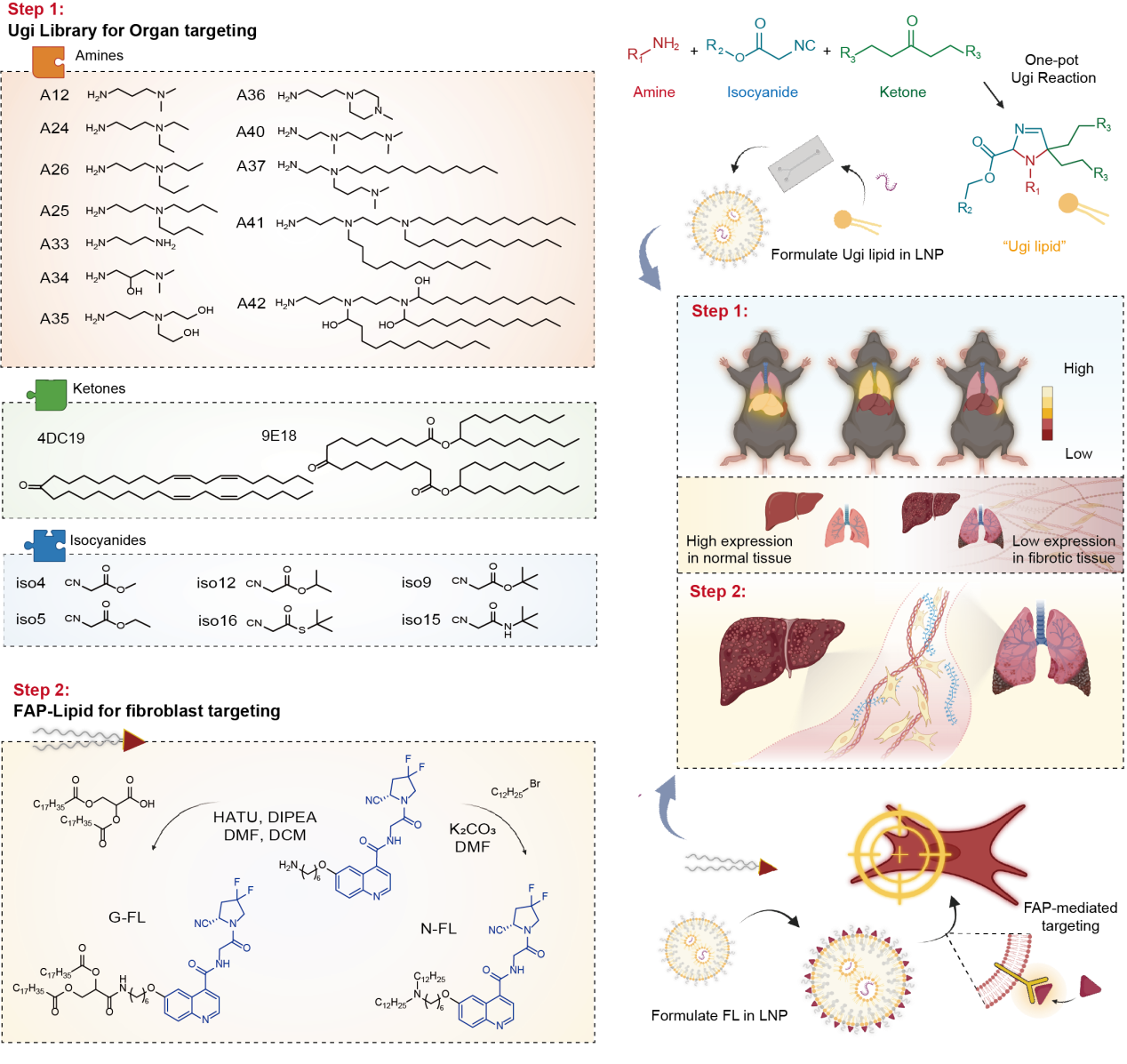
�D1. �_�l�w�S�����ٺͼ����fͬ�����f��ƽ�_��FOCUS LNPs�����������w�S���^���mRNA�f��
ԓ�о��ĵ�һ��Ɇ�λ�DZ�����Wˎ�WԺ��Ȼˎ�P����ˎ��ȫ�����c����ҡ�������Wˎ�WԺ�����о��T��ɽ�|��W�R���tԺ��쳸�����ˎ����ԓՓ�ĵ�ͨӍ���ߡ�κ�������������S����Փ�ĵĹ�ͬ��һ���ߡ���Ȼˎ�P����ˎ��ȫ�����c����҃x��ƽ�_�ͱ�����W�t�W���tˎ�l���������ĵĸ�λ�ώ���ԓ�о��ṩ����Ҫ������ԓ��о��õ�������Ȼ�ƌW���𡢱����п�ί��������Ȼ�ƌW����Ȼ����Ŀ��֧�֡�
Փ��朽ӣ�https://pubs.acs.org/doi/10.1021/jacs.5c16886
ͨӍ���ߺ��飺

���٣���ʿ���о��T��������W��������W�ߣ�������Wˎ�WԺˎ��ϵ����Ȼˎ�P����ˎ��ȫ�����c����ҡ�������W-���ϰ�ˎ���H�t�W�о������������ڣ����Ҽ��˲�Ӌ�������Ŀ���x�ߣ������և������c�аlӋ����������Ȼ�ƌW������Ŀ������Ŀǰ����ԓ�I��l��SCIՓ��43��ƪ������ͨӍ����һ����(����ͬͨӍ��һ��)Փ��23ƪ������Nat Biotechnol��Nat Commun��3ƪ����Sci Transl Med��JACS��2ƪ����Cell Rep Med��Cancer Res��ACS Nano��Adv Funct Mater��Adv Sci��Adv Healthc Mater��Adv Drug Deliv Rev��Mol Cancer��J Controlled Release�ȣ�Փ��SCI���ôΔ�4000��Ρ��о��ɹ���피�ˎ�W�����W�C���ڿ������c��B������l����֮һ���ڙ�PCT����2헣����P֪�R�a�༰�о��ɹ����D������֪��������ˎ��ITranslate Bio�������tˎ��˾OncoTrap��Qualiber���ڿ��[�����缰�[���h���{�������о��c�_�l��
��һ���ߺ��飺

κ������������Wˎ�WԺ2025����ʿ�����о��dȤ�����Ϳ���x��x��֬�|����OӋ�c�_�l������Ŀǰ���Թ�һ���߰l��Փ��1ƪ��

����������Wˎ�WԺ2022����ʿ�����о��dȤ���w�S�����P�����İ����c�����ί�������Ŀǰ���Ե�һ/��һ����Փ��7ƪ������Nat Commun (2ƪ)��JACS��J Controlled Release (2ƪ)��J Nanobiotechnol��Chem Eng J����Ո�l������4헣��@��1헡��Բ�ʿ��W�ԁ����@�ñ�����WУ�L���W�����ÌW�����W�g���ª��Șs�u�Q̖���@������Ȼ����W�����A�о��Ŀ����ʿ�о��������͡��Ї��ƅf���й��̲�ʿ�����Ӌ�����Y����

�S���������W��ʿ���s�����ս�˹��W�Tʿ��������ʡ�����WԺRobert Langer��������֬�|�w�{���w����LNP�����g�����¹����鱬�lǰ���Թ�ͬһ����Nature Biotechnology�ϰl����������֬�|�w��mRNA�����о����I��ȫ���S��LNP���g���¹������еďV�����ã����о����ܲ�Ŀ�����l�˱�����֬�|�w�Ͱ��Y�������о���������600�Ρ�Ŀǰ��Nature Biotechnology��Advanced Materials��Nature Communications��Nature Materials��JACS��Applied Physics Letter���ڿ��l��Փ��17ƪ����Ӌ�����ó��^1800�Ρ�
��Ȼˎ�P����ˎ��ȫ�����c�����