
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
�����A���tԺ�����ί��о�������Դ/�����о��T�F���Cancer Discovery�l�Ľ�ʾ�z�|ĸ�������Ͱl�C�ƺͰ������
�����w�� �� �� С �� �r�g��2026��02��28�� ��Դ���Ĵ���W�A���tԺ
�����]��
����2��27�գ��Ĵ���W�A���tԺ�����ί��о�������Դ/�����о��T�Fꠣ������A��W/�����P�����R�����������Ƽ�������W�����A�Fꠣ����[���W���H피��ڿ�Cancer Discovery��IF:33.3���ھ��l���}�顰Glioblastoma-secreted C1QL1 orchestrate...

2��27�գ��Ĵ���W�A���tԺ�����ί��о�������Դ/�����о��T�Fꠣ������A��W/�����P�����R�����������Ƽ�������W�����A�Fꠣ����[���W���H피��ڿ�Cancer Discovery��IF:33.3���ھ��l���}�顰Glioblastoma-secreted C1QL1 orchestrates tumor microtube expansion and neural synaptic pruning to drive malignant synapse formation and recurrence�����о�Փ�ģ��l�F�z�|ĸ��������GBM�����ڵ�C1QL1�ǽ錧�[�����[�����[������ԪͨӍ���P�I��̖���ӣ�����C1QL1-BAI3-Rac1��ͬ�r���TM�͐���ͻ�|�γɡ������[���Ͱl��
�Ĵ���W�A���tԺ�鱾Փ�ĵ�һ���߆�λ�͵�һͨӍ���߆�λ�����A��W/�����P���������ڡ����t�ƴ�W�����쉯�tԺ�������ڞ鱾�о��ṩ�˴���֧�ֺ͎�����
�z�|ĸ��������GBM�����Ҋ�����Գ̶���ߵ�ԭ�l���X�[���������A��O�GBM�ʬF�V���Ľ��������L�������^�[�������y��ͨ�^���g+�Ż������������ˎ�͏Ͱl����Ҫԭ������о�������GBM���������u��ʼ�A�λ������B�����ڶ�ֲ������L����ͻ�ӵ��[���ܣ�TM����B���γ��[���W�j�����c������Ԫ�γɹ���ͻ�|������ͻ�|����������Ӯa�������̖���Է�����̖���M�[�����L����ˎ�͏Ͱl��Ȼ���������^�z�|���������ͨ�^�[�������gͨӍ���MTM���[���W�j�γɡ�����c����ͻ�|�����γɐ���ͻ�|�ķ��әC���в������������̖�����в����_��Ҳȱ����Ч�ĸ��A���ԡ�
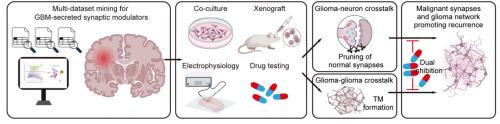
�о��F����϶�MGBM�μ����c���g�D䛽M�������l�FC1QL1���[�������^��늻�ӵ�GBM OPC-like�������خ��Ը߱��_���c���߲����A�̏Ͱl�r�g���P���ڶ�NGBMģ�����C������P�I�ٰ����ӡ��Mһ���о�������C1QL1 �{���[�����[������Ԫ���������M�[�������gTM�γɡ�������Ԫͻ�|������Ԫ���z�|������ͻ�|�γɡ��C���ϣ�C1QL1�cGBM��������Ԫ��BAI3���w�Y�ϣ�����Rac1��̖���M�����Ǽ����ţ���GBM���T��TM�γɣ�����Ԫ���T��ͻ�|�����M���ƄӐ���ͻ�|�γɡ�
���A��W/�����P�������/�R�����F�ǰ���_�l��һ����aFirst-in-class ��GEF�����Rac1���Ƅ�JK50561�����^���ш����Rac1���Ƅ����и�Ч�Ͷ�����Ѫ�X����ͨ�Եȃ��ݣ�Ҳ��Ŀǰȫ��Ψһ��ɰ�Ɲ��Ĭ�Y�ί��R������ԇ��Rac1���Ƅ����R�������@ʾ���õİ�ȫ�Ժ���Ч�ԡ��о��Fꠜyԇ�l�FJK50561����Ч����GBM��TM���γɣ����GBM�T������ͻ�|�������Ɛ���ͻ�|�γɡ���GBM�g��Ͱlģ����Ҳ�������[���Ͱl�����L�����ڣ�߀��������Pͨ·���[�����P��Ԫ������ӣ��c�ů��ÿɅfͬ���ƏͰl��
�C�ϣ����о��l�FC1QL1��������^GBM�������ڵĺ�����̖���ӣ�ͨ�^�����[���W�j��TM�γɣ��������h·����ͻ�|�������p��������GBM�Ͱl����ʾ�˽����^GBM���{���C�ƺͰ�����ԡ�
ԓ�о��@�Ç�����Ȼ�ƌW���𡢇��ҿƼ������c�аl���Ĵ�ʡ�Ƽ��d���A���tԺ��1��3��5��Ӌ���ȶ�헻���֧�֡�
ԭ��朽ӣ�https://doi.org/10.1158/2159-8290.CD-25-1123