
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
�����WԺ�R���F��c�����߽�ʾTHAP1���{��С����̥��һ��DNA���Ƶ�ĸԴЧ������
�����w�� �� �� С �� �r�g��2026��03��01�� ��Դ�����A�@�����WԺ
�����]��
�����ڲ���������ڰl���У���ĸ�����ڳ���ǰ���e�۴���ĸԴ�����|�cRNA�����ܾ���ĸԴ-�����D׃�� ��Maternal-to-Zygotic Transition, MZT�����S��l����ZGA�ṩ���A��ĸԴЧ������Maternal Effect Genes��MEGs���������б��_�ͷe�ۣ��������ӳ����A�β�һ�����й��ܡ����ܾ�����̥�l���^���Єt�l�]�P�I���á�֮ǰ�l�F��ĸԴЧ��������c���^�z���{�ػ�RNA���x���P��������̥�ĵ�һ��DNA����ͨ���l���ڻ���M����֮ǰ�����ĸ...
�ڲ���������ڰl���У���ĸ�����ڳ���ǰ���e�۴���ĸԴ�����|�cRNA�����ܾ���ĸԴ-�����D׃�� ��Maternal-to-Zygotic Transition, MZT�����S��l����ZGA�ṩ���A��ĸԴЧ������Maternal Effect Genes��MEGs���������б��_�ͷe�ۣ��������ӳ����A�β�һ�����й��ܡ����ܾ�����̥�l���^���Єt�l�]�P�I���á�֮ǰ�l�F��ĸԴЧ��������c���^�z���{�ػ�RNA���x���P��������̥�ĵ�һ��DNA����ͨ���l���ڻ���M����֮ǰ�����ĸԴ���ӌ�����̥��һ��DNA�������P��Ҫ��
2026��2��23�գ����A��W�����ƌW�WԺ�R�������c�㽭��W�t�WԺ���t�W�z���c�l���о�Ժ����������ڈF����ڡ�EMBO��桷��EMBO Reports���ڿ����L����ʽ������}�顰ĸԴЧ������THAP1ͨ�^Rrm1�{��С��������̥�ĵ�һ���������ڡ���THAP1 is a maternal effect factor required for the first cell cycle via Rrm1 in early mouse embryos�����о�Փ�ġ��о��F꠰l�F���D�����THAP1����ĸ�����б��_���������Rrm1�ڃȵ��ٔ����P�I�Ļ���RRM1���cdNTP�ϳɣ����������еķe�۱��C��������̥���ܾ����һ��DNA���Ƶ������M�С���ĸԴTHAP1ȱʧ�r����̥1����DNA�����M���@�����t�����F1�C2�������Ӿ��������ͬ�r���S���ӻ���M���Zygotic genome activation, ZGA��ȱ�ݣ���K���´��������������½���
THAP1����Thanatos���P�����壬�Ǻ�THAP�Y������D����ӡ�������У�THAP1����ͻ׃�����lһ�N��ϵ�y�\���ϵK�����������ϵK6�ͣ�DYT6����Fuchs et al., 2009�������^�ڷֻ��ĽM����THAP1���������Ӻ�����ǰ��̥�б��_�ܸߣ�������������̥�l���еľ��w�����Բ���������@�@һ���}���о��Fꠘ�������ĸ�����خ���Thap1ĸԴ�ó�ģ�͡��Y���@ʾ��ĸԴThap1ȱʧ����ĸ�����l���ͳ��첢�o�@��Ӱ푣����ܾ�����̥��1������2�����İl���M�����@���t���S����̥ͣ����1�C2�����A�Σ������S���ӻ���M����ȱ�ݣ���K��ɴ����������@���½���
���������ӻ��A���о��FY���D䛽M�����l�F��Thap1ȱʧ��������ĸ������һС���ֻ�����_���{�����а������a���Ǻ�����߀ԭø������Rrm1��RRM1���cdNTP�ϳɣ���DNA������������P�I�h�������C��Thap1�ó���dNTP��Ӱ푣��о��߲��Ã����ğo��ӛHPLC-MS���ԣ��L���˸��w��ĸ�������L���ܾ������ں��ӵĴ��x�ӑB�D�V����ĸԴThap1ȱʧ�����£������A��dNTP���o�ܵ�Ӱ푣��M������1��������̥S���˳����t��DNA�p�������Լ��������ڙz���c���m�����K����1������2�����İl�����������Mһ���C��Rrm1�cdNTPֱ��Ӱ���̥�l�����о��F�ͨ�^�ں������^���_Rrm1���܉��@������ĸԴThap1ȱʧ��̥�İl���M�̣�ʹ2�����M���cZGA�ڎ��õ���ȫ�֏ͣ��a��Rrm1���a�dNDPs����Ɍ����Pȱ�ݮa��һ���̶Ⱦ��⡣�����Y����֧ͬ�֡�THAP1-Rrm1-dNTP���o�����ܾ����һ�����������е��P�I���á�
�C�ϣ�ԓ�о����D�����THAP1�_����С�����ڰl���^���е�ĸԴЧ������֮һ����ʾ��ͨ�^�{�غ�������x���P������_���������е�һ��DNA���ƣ��D1����
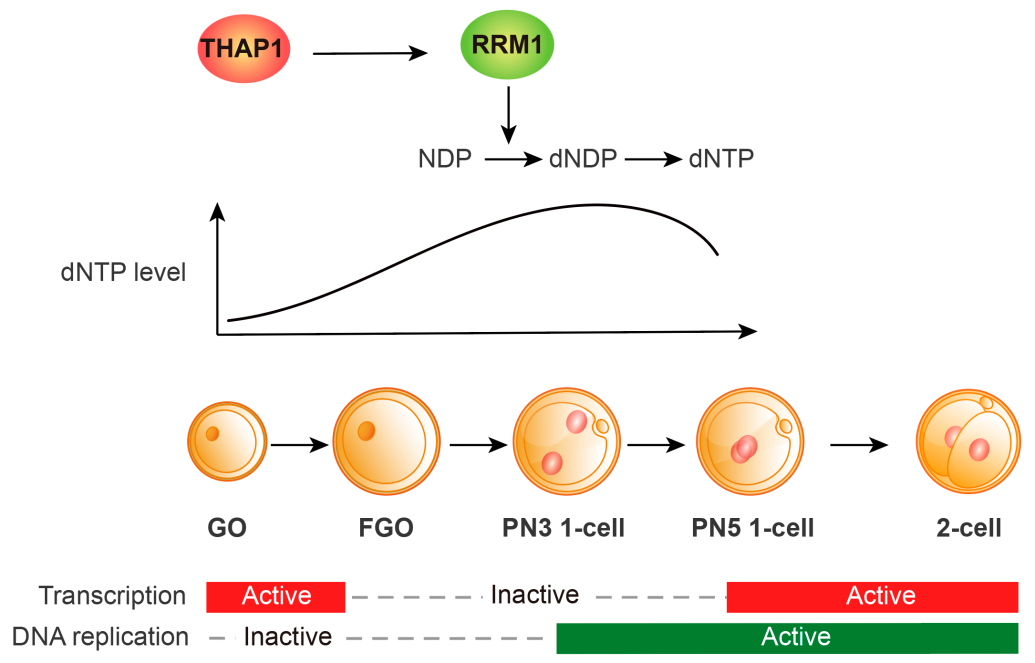
�D1. THAP1ͨ�^�D��{�����λ���Rrm1�������ܾ����һ��������������dNTP������֧��1������2�����D׃�����ӻ���M���ZGA��
���A��W�����ƌW�WԺ�R�������c�㽭��W�t�WԺ���t�W�z���c�l���о�Ժ����������ڣ�ԭ�R���M��ʿ��Փ��ͨӍ���ߣ����A��W2024�ò�ʿ���I��������������WPTN�Ŀ2020����ʿ����ϣ�����A-���������ƌW�����IJ�ʿ���h���Ȟ鹲ͬ��һ���ߡ����о��õ��»�ʯ�о��T�������A��W���������ĺ����A��W����Ӌ�����ĵ�֧�֣����@�Ç��ҿƼ������c�аlӋ����������Ȼ�ƌW����������A-���������ƌW���ĵȽ��M֧�֡�
Փ��朽ӣ�https://doi.org/10.1038/s44319-026-00712-9