
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
κ�F��_�l���ڲ����ں��ĵ�LNP�f��ƽ�_�����FmRNA��Ч�����f��
�����w�� �� �� С �� �r�g��2026��03��02�� ��Դ���Ї��ƌWԺ�����о���
�����]��
����֬�|�{���w����Lipid Nanoparticle��LNP���F�ѳɞ��w��mRNA�f�͵��������g���ڂ�Ⱦ�����硢����������������Y�ί����������I��չ�F���ˏV韵đ���ǰ����mRNA-LNP��Ҫͨ�^����;���M�뼚���������D�\�����ڃ�...
֬�|�{���w����Lipid Nanoparticle��LNP���F�ѳɞ��w��mRNA�f�͵��������g���ڂ�Ⱦ�����硢����������������Y�ί����������I��չ�F���ˏV韵đ���ǰ����mRNA-LNP��Ҫͨ�^����;���M�뼚���������D�\�����ڃ��w�С���mRNA��Ҫ�ă��w�����������|�в��܉��g��Ŀ�ĵ��ס�Ȼ������ǰLNP�ă��w���������ձ鲻�㣬�@�����Ƽs��mRNA�������ί�Ч����
2026��2��19�գ��Ї��ƌWԺ�����о���κ�F��ڡ�Advanced?Materials����IF=26.8���ϰl�����}�顰?Fusion Peptide-Incorporated Lipid Nanoparticles Boost Endosomal Escape and Enhance Cytosolic mRNA Delivery�����о�Փ�ġ�ԓ�о������Ѓ��H�ԵIJ�����Դ�����˹��ϳɵ��ں��ķ��b��LNP�Ȳ��������˻����ں��ĵ�LNP��Fusion Peptide-LNP��FP-LNP��ƽ�_���D1����ԓ�����@��������LNP���f��Ч�ʣ����У���Դ�����в�����HA2�ں������w��������F�����mRNA�f������Ч�����C���о�������HA2�����벢δ��׃LNP�ļ����zȡЧ�ʻ��w�����ٷֲ�������ͨ�^�������wĤ�_��������mRNA���w���݁����mRNA-LNP���f��Ч�ʡ�
�о��F��Mһ��������ԓ���Եđ��ÏV���ԣ���HA2�ں��������N�ΰ���LNP�Լ�������K��Ƣ�K�����ٰ���LNP��SORT LNP���У����^�쵽mRNA�f��Ч�ʵ��@��������HA2-LNP���f��Cas9 mRNA��sgTOM���Ԍ��F���K�ͷ��K�и���Ч�Ļ��������z�����Ұ���Ѫ�YI�ͣ�HT-1��С��ģ�͵ĵ�����������о��У��c��ҎLNP��ȣ�HA2-LNP���@���p�p�˸��K�w�S�����װY���������F�����@�����ί����ݡ�
ԓ�о�ͨ�^�������ں�������mRNA-LNP���ɹ��_�l��һ�N���m����Ч�IJ��ԁ�ͻ��mRNA�����ă��w����ƿ�i��ԓƽ�_���H�c�F�ж�NLNP�䷽���ݣ����ڻ����͵������������չ�F���������ί�����������һ����ЧmRNAˎ����_�l�ṩ���µ�˼·��
�Ї��ƌWԺ�����о���κ���о��T��ԓՓ�ĵ�ͨӍ���ߣ��Ї��ƌWԺ�����о�����ʿ�о����Ɂ�骞��һ���ߡ�ԓ�о��õ����Ї��ƌWԺ�������Ȍ���헡�������Ȼ�ƌW������Ŀ�Y����
����朽ӣ�https://doi.org/10.1002/adma.202515130
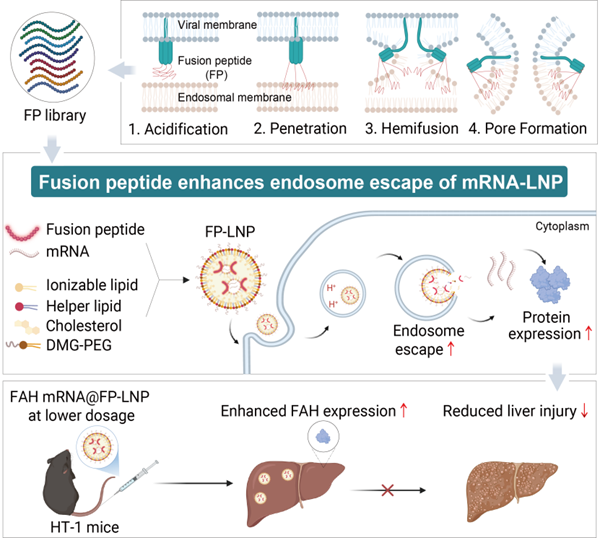
�D1. �����ں������mRNA-LNP�ă��w���ݺ��f��Ч��