
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
�������о��M�_�lNKP�[���ί��¼��g
�����w�� �� �� С �� �r�g��2026��03��02�� ��Դ���Ї��ƌWԺ�����о���
�����]��
����CAR-NK�����ڼ����ί���չ�F����ȫ��ͨ�õă��ݣ�����Ч�����롣�R���ϣ��������CAR-NK������Ч������ø߄�����������ݔע�oˎ�IJ��ԣ��@�����ί��ɱ��@�����ӣ����ػ��߽���ؓ������ˣ����y�����w�M����ԴCAR...
CAR-NK�����ڼ����ί���չ�F����ȫ��ͨ�õă��ݣ�����Ч�����롣�R���ϣ��������CAR-NK������Ч������ø߄�����������ݔע�oˎ�IJ��ԣ��@�����ί��ɱ��@�����ӣ����ػ��߽���ؓ������ˣ����y�����w�M����ԴCAR-NK�����������R��Ч�ͳɱ����}�p������
2026��2��24�գ��Ї��ƌWԺ�����о������������c����ȫ�����c������������о��M�ڸɼ����I�I����Cell Stem Cell���L����ʽ�ھ��l�����}�顰Pluripotent stem cell-derived CAR-NK progenitor therapy targets minimal residual disease and prevents relapse in leukemia models���������о��ɹ����D1�����о��F��_�l�����ܸɼ����T����Դ��CAR?iNK�棨CAR-iNKP���������������F�w�ȴ�Ҏģ�a�����m�r�g�õ�CAR-iNK���������y�����ϵ̈́�������һ���ε�CAR-iNKP����ݔע�Ϳ������B-ALL��T-ALL�[������ģ���ό��F��Ч����[��С��������@�������[���Ͱl�ʡ�ԓ��о��ɹ�����yCAR-NK�����������R���w�ȴ��m�r�g�̡��L�گ�Ч����Ȇ��}�ṩ���¼��g��Q·����
�L���ԁ����������о��M�������_�l���w�����N���w�Ȱl�����족�ăɲ�������ѪҺ/���������ԣ���������Һ������ġ���������B������Ҏģ�Ƃ�iNK�����ļ��g��ˇ��ԓ�о�ͨ�^����������Bϵ�y�T��iNK���������wϵ�_չ�μ������e�ĕr�ՄӑB�������ɹ��b�����c��ȻNKP������Virginie M. Renoux, et al. 2015 Immunity�����ͺ������Ƶļ���Ⱥ�w�������䶨�x��iNKP������
�S���о��ˆT�����˱��_CXCR4��CXCL12���w����hPSC��R4-PSC������ϵ�����w���T����ֻ��@�þ��й���w��������NK�����N�ӡ�R4-iNKP������ͨ�^β�o�}ݔע�̈́���R4-iNKP������IL15��Դ��С��B-NDG hIL15С��20�fR4-iNKP/ֻ���������w�������裬��7-10���ڹ����h���аl�������R4-iNK���������M��ѪҺѭ�hϵ�y���K���ܰͽY��Ƣ�K�����K�ȶ������w�K�������˹�����ǣ��@�N�w���������Ԍ��FiNK����������ѪҺѭ�hϵ�y���m����80�����ϡ����_CAR��R4-iNKP����ͬ�����w�Ȯa��CAR-R4iNK����������������ѪҺѭ�hϵ�y�д��ڳ��^80�죨�D2����
�����u��CAR-R4iNKP�����ί��[�����D���������о��ˆT�x����CAR-T�����ί��I��Ľ�����cCD19��CD7���քe�yԇCAR-R4iNKP����������B���ܣ�B-ALL����T���ܣ�T-ALL���[����Ч�����о��ˆT���ȜyԇCAR-R4iNKP�����w�Ȯa����CAR-R4iNK�����ܷ��A���[���l������B-NDG hIL15С����ݔע20�f��CAR?R4iNKP��������2~3�ܺ���ע��CD19��Ե�NALM6�[��������CD7��Ե�CCRF?CEM�[��������ģ�M�[���l���������Y�����������Ќ��MС����ɹ������[���ӷN���𣬶�δݔעCAR?R4iNKP�Č��սMС��ȫ���l���[������ˣ��w�ȷֻ��a����CAR?R4iNK�����܉���Ч�ֿ��[���ӷN�����𣬾߂�һ���ľ������߱Oҕ�[���l���Ĺ��ܡ�
������Ͱl���R���ί������[����ʹ�c�����u��CAR?R4iNKP��������������[��С�������MRD���ĝ�����ԓ�о��M���˻�����CAR-R4iNKP����ݔע�������MRD�ĸ�����C���Y���@ʾ�����ϵ̈́�������һ���ε�CD19CAR?R4iNKP����ݔע�����������B-ALL�[������ģ���ό��F�L����Ͱl��ͬ�ӷ���Ҳ�Ɍ��FT-ALL�[���Ͱl�ʽ���50%��ʣ���ͰlС���������Ҳ�@�����L���H���ܻ����������ϲ���CAR��R4?iNKP��������ݔע�����CAR?R4iNK������ϵ�Ќ��սM�����F100%�[���Ͱl���C�ϣ�CAR?R4iNKPݔע������w�Ȱl��������CAR?R4iNK�������ϻ�������Ч���MRD���@�������[���Ͱl�ʡ�
���������T����ӛ����NK��memory-like NK, MLNK��������һ�IL-12��IL-15��IL-18�̕r�A�����a���ľ�������ӛ��������NK������Ⱥ�����w�ȳ־����@�����ڂ��yNK������Rizwan Romee, et al. Blood, 2012; Rizwan Romee, et al. Science translational medicine, 2016����ԓ�о����^�˽���������Ѫ�Ƃ��CAR-NK��Auto-PBMC-CD19CAR-NK��������CAR-MLNK��Auto-PBMC-CD19CAR-MLNK��������ͬһ��iPSC��Դ��iPSC-CD19CAR-R4iNKP����ݔע�ί��[����Ч�����Y���@ʾ��iPSC-CD19CAR-R4iNK�������w�ȳ־��Ծ��@������Auto-PBMC-CD19CAR-NK������Auto-PBMC-CD19CAR-MLNK���������ϻ�������[��MRD���棬iPSC-CD19CAR-R4iNKP����ݔע�M��С��@�����L�ھ��⣬������Auto-PBMC-CD19CAR-NK������Auto-PBMC-CD19CAR-MLNK����ݔע��С������F�[���Ͱl���@һ�z���W��֔���սY���Mһ���C��CAR-iNKP�����˷��˂��yCAR-NK�������w�ȴ��m��ƿ�i��
�о��F��^С��iT������iB�����Ͷ�ѪҺ�����Vϵ�w�������ɹ��������NK���������I���ٴ��C�����w�����N���w�Ȱl�����족�ɲ����������Ե�ͨ���ԡ�ԓ�ɲ������Ԟ�δ���_�l����ɼ�����Դ�����ѪҺ�������漚���Ƅ����_չ�R���D���yԇ�ṩ����Փ֧�֡�
�Ї��ƌWԺ�����о����������ɼ����c�����t�W�о�Ժ�������о��T��Փ�����ͨӍ���ߡ������ɼ����c�����t�W�о�Ժ�����Ը��о��T���Ї��ƌWԺ�����о��������Ƹ��о��T����ͯ�����о��T��Փ�Ĺ�ͬͨӍ���ߡ���ͬ��һ���߰������Ї��ƌWԺ�����о�����ʿ�о�������Ǭ���������������ɼ����c�����t�W�о�Ժ���о��T�S�ºƺ��ij��飬�����̎��̆�ͯ���Լ��Ї��ƌWԺ�����о�����ʿ���I�������p��ԓ�о��ڇ�����Ȼ�ƌW����ԭ��̽��Ӌ���Ŀ��82450001�����������c�аlӋ����2024YFA1108302���������l��ί�Ĵ������ش�헣�2023ZD0501200�����Լ�������Ȼ�ƌW���������ĿC������Ŀ��82300132��32300676��82470120����ͬ�Y������ɡ�
ԭ��朽ӣ�https://doi.org/10.1016/j.stem.2026.01.013
�P�I�~��PSC, CXCR4, CAR-iNKP, MRD

�D1
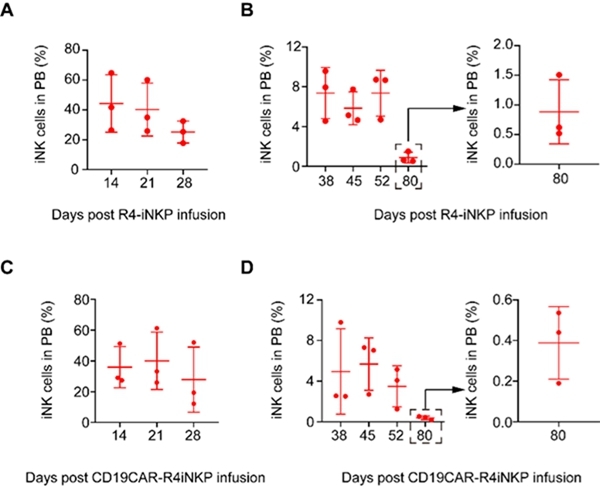
�D2?iNK/CAR-iNK�������w�ȵĴ��m�r�g���^80��
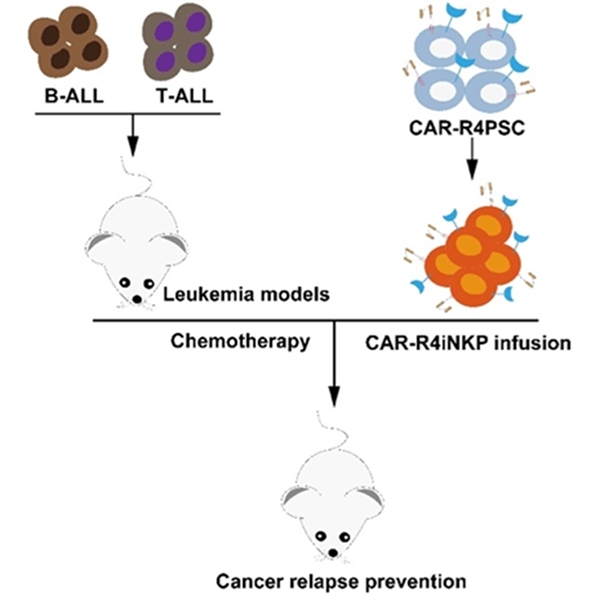
�D3 CAR-iNKP��������ʾ��D image by WANG Jinyong lab