
-

����ͨ��
����ץס�����Ƽ�
���ӵ��}��
Bioactive Materials | ���ԳɈF��_�l���w��Ƣ�KDC���������mRNAˎ���f��ϵ�y
�����w�� �� �� С �� �r�g��2026��03��03�� ��Դ��������W�t�W��
�����]��
���� ? ? ?2026 �� 2 �� 18 ��,������W���ڡ� ��������ˎ���о�Ժ �߶�ˎ���Ƅ��cˎ�ò����о�������ϯ�ƌW���� �� �ɈF��ڇ��H�W�g�ڿ� Bioactive Materials �ھ��l�����}Ŀ�� Splenic dendritic cell-targeting mRNA transfection of H-type ionizable lipid-based LNPs for enhancing tumor immunotherapy �� �����о��ɹ� ,ԓ�о��_�l��һ��� H �Y���Ŀ���x֬�|,��ԓ֬�|�Ƃ�� LNPs �Ɍ��F mRNA ˎ�����w��Ƣ�K DC �� ���İ������f��,���[�� mRNA ������_�l�ṩ���²���
? ? ?2026��2��18��,������W���ڡ���������ˎ���о�Ժ�߶�ˎ���Ƅ��cˎ�ò����о�������ϯ�ƌW�������ɈF��ڇ��H�W�g�ڿ�Bioactive Materials�ھ��l�����}Ŀ��Splenic dendritic cell-targeting mRNA transfection of H-type ionizable lipid-based LNPs for enhancing tumor immunotherapy�������о��ɹ�,ԓ�о��_�l��һ���H�Y���Ŀ���x֬�|,��ԓ֬�|�Ƃ��LNPs�Ɍ��FmRNAˎ�����w��Ƣ�KDC�����İ������f��,���[��mRNA������_�l�ṩ���²��ԡ�
��Щ���,mRNA�������T�༲���ί��I���ѳɞ�һ�N�����Ե��ί��ֶΡ�����,��֬�|�{���w��(Lipid Nanoparticles, LNPs)����mRNA�f���d�w���ڸ�Ⱦ�Լ���(��COVID-19��RSV��)���A����ȡ���@���ɹ���Ȼ��,���[�������ί��I��,��Ό�mRNA�����f����Ƣ�K�@һ�P�I��������,�e�ǰ������еĘ�ͻ���(DC),�Ը�Ч����C�w�خ��Կ��[�����ߑ���,����һ��ؽ����Q������
�p������x��֬�|��һ��Ƀɂ�����늺ɵ��^�����F�̓ɗl��ˮ�����β�ͨ�^�B���۽Y�����ɵ����H������,�����ں���ˎ���f��ϵ�y�Ę�������ԓ�F�ǰ���о���,�OӋ��һ�N��ه�����^�����F�̓ɗl����β�ͨ�^�����I��Ӷ����p������x��֬�|(ssGLCL)(J Control Release. 2016, 235:99-111)�����Y������,ԓ֬�|���w����w�Ⱦ�չ�F��������siRNA�f��Ч�ʡ�����,siRNA/ssGLCL��x�Ӽ{�ͺ����܉��γɾo�ܶѷe�Ķ������ݽY��,�@�N����Y�����H�������z�w������,߀����Ч���osiRNA���ܺ���ø�Ľ��⡣
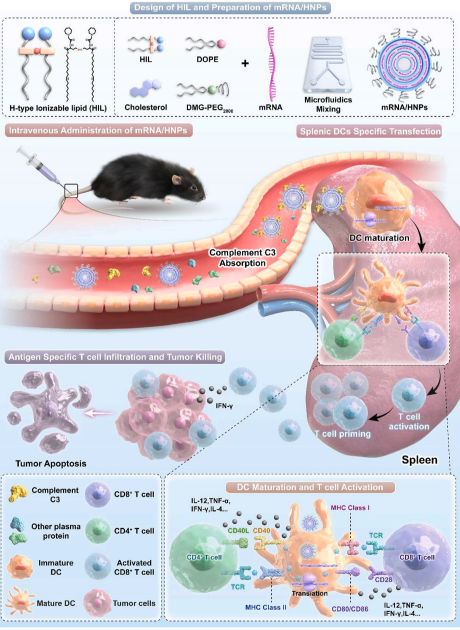
�D1 mRNA/HNPs���Ƃ䡢�w�����\�����[���C��ʾ��D
�ڱ��о���,ԓ�F���ǰ�ڹ������A,�OӋ��������һ������p���Ϳ���x֬�|��(H�Ϳ���x֬�|,H-type ionizable lipids),����ʮ�N��ͬ���尷�^�����F�̓ɷN�����オ����B�ӱ�,ּ�ڌ��FmRNAˎ����w�ȸ�Ч�f�͡�ͨ�^ϵ�y�Y�x�c̎������,��K���x�õ�mRNA/H18NPs�������R�Y������,ԓ�{���w�����Ъ��ص�ͬ�Ķ��ӽY���������Ԍ���@ʾ����ϡl����Ѫ��h���о����F�������ķ����ԡ���D1��ʾ,���o�}ע���,mRNA/H18NPs�o����������w���Ɍ��FƢ�K��ͻ���(DCs)���خ����DȾ. ����Ƣ�KDC���DȾЧ��������mRNA/MC3-LNPs��1.84�����Mһ���ęC���о�����,mOVA/H18NPs�܉�ͨ�^������γɵĵ����и������a�wC3����,�錧�@�NƢ�KDC���خ��Ԕzȡ�c�DȾ��C57BL/6JС��ģ����,�o�}ע��ɴ�mOVA/H18NPs���@������Ƣ�K��OVA�خ���CD8+ T������IFN-��+ CD8+ T�����ı���,�քe��OVA/MC3-LNPs�M��6.9����3.1��,չ�F�����ҵ���������������NС���[��ģ��(B16-OVA��B16F10)�еČ��Y������,mRNA/H18NPs�܉l��Ч�Ŀ�ԭ�خ������ߑ���,չ�F���@���Ŀ��[����Ч:��B16-OVA��B16F10�[��ģ�͵������ʷքe���_95.9%��94.6%,������Ч�����[����β��D�ơ�ֵ��ע�����,�����A��������,mOVA/H18NPs���F��Խ���[���A������,��ʹС����180��������ʾS��100%��ԓ���Ԟ��[�������ί��ṩ���µ�˼·�c�ֶΡ����P�о��ɹ�����Ո����(2024103472188��PCT/CN2024/135192)



��������:��������Z�x
ԓ�о��ĵ�һ��Ɇ�λ�DZ�����Wˎ�WԺ��Ȼˎ�P����ˎ��ȫ�����c����ҡ�������Wˎ�WԺ���Գɽ��ڞ�ԓՓ�ĵ�ͨӍ���ߡ�2021����ʿ�о�����Ρ�2023����ʿ�о�������Co-PI�Z�x���о��T��Փ�ĵĹ�ͬ��һ���ߡ��F꠳ɆT������,���Խ,Ѧ����,�״���,���\,�ǵ�,���Ԏr�ώ�����Ԫ܊���о��T��ԓ�о���������Ҫؕ�I����Ȼˎ�P����ˎ��ȫ�����c����҃x��ƽ�_��������W�t�W���tˎ�l���������ġ�������W��������ˎ���о�Ժ�ĸ�λ�ώ���ԓ�о��ṩ����Ҫ������ԓ��о��õ�������Ȼ�ƌW���𡢱�������Ȼ�ƌW�����������c�аlӋ���Ȼ����Ŀ��֧�֡�
Փ��朽�:https://doi.org/10.1016/j.bioactmat.2026.02.018
ͨӍ���ߺ���

���Գ�,������W������Ƹ����,ˎ�WԺˎ���Wϵ����,��ʿ������,������W���в������L���t�W������̎̎�L,������W��������ˎ���о�Ժ��Ժ�L,�������L���W����Ƹ����,�Ƽ���������Ƽ������I܊�˲š������������o�����˲�,�����пƼ����ǡ��F���Ї�ˎ�W������ˎ��Iί�T��������ί�T���Ї�ˎ�W��ˎ�����Iί�T��ί�T������ˎ�W��ˎ�����Iί�T������ί�T���о�����۽���������ˎ��oˎϵ�y�о��������Լ{��ˎ���f��ϵ�y�о���ؓ؟���և�����Ȼ�ƌW����7�,�Г�����mRNAˎ�����c�аlӋ���Ŀ�������ش���ˎ���ƃ�ͯˎ�аl���gƽ�_�ȇ��Ҽ���ʡ�����Ŀ6�,�l��W�gՓ��140��ƪ,���g�������{����ˎ��ݔ��ϵ�y����