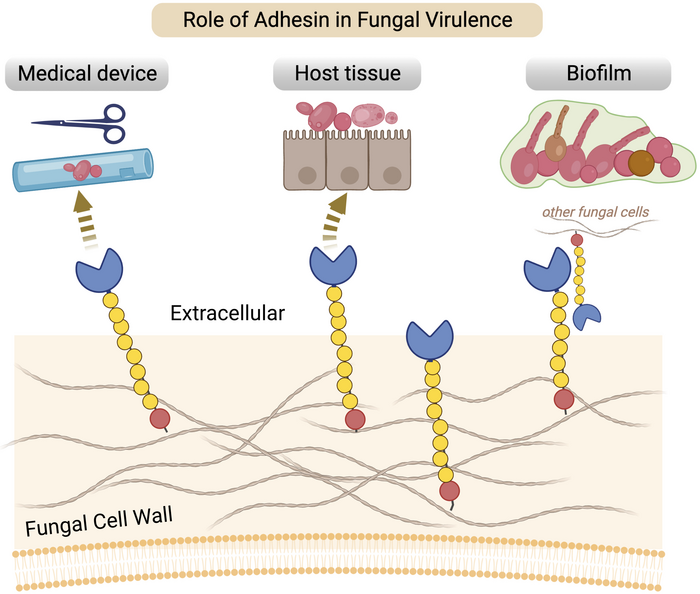
圖片:愛荷華大學(xué)的生物學(xué)家在致病真菌中發(fā)現(xiàn)了一個共同的遺傳因素,其中包括一個與美國醫(yī)院疫情有關(guān)的物種。該圖像顯示了Hil基因家族編碼的蛋白質(zhì),這些蛋白質(zhì)扎根于細胞中,并利用粘性或粘附性將自己附著在導(dǎo)管等醫(yī)療設(shè)備上,附著在組織上,或創(chuàng)建一種稱為生物膜的耐藥壁。
大自然有一種巧妙的方式來利用有利的情況。
以假絲酵母菌為例。這種酵母在2009年還不為人知,但當科學(xué)家們了解到它會對醫(yī)院和護理機構(gòu)的病人造成危及生命的侵入性感染時,它突然出現(xiàn)在了人們的視野中。2019年,金耳錐菌的危險非常嚴重,以至于美國疾病控制和預(yù)防中心將其列為嚴重的全球健康威脅,理由是這種酵母的傳播及其對許多抗真菌藥物的耐藥性。上個月,疾病預(yù)防控制中心報告說,美國近一半的州都發(fā)現(xiàn)了金黃色葡萄球菌
那么,一種簡單的未知酵母是如何突然成為公眾健康的敵人的呢?愛荷華大學(xué)(University of Iowa)的生物學(xué)家說,部分答案是在一個編碼粘性特性的基因家族中找到的,這種基因家族似乎是真菌疾病毒性的核心,包括一些威脅人類的疾病。
在一項新的研究中,研究人員報告了一個這樣的粘著蛋白家族,稱為Hil家族,存在于所有酵母物種的共同祖先中,但在致病物種中比良性物種中數(shù)量更多。此外,研究人員還發(fā)現(xiàn),一些具有大型Hil基因家族的致病物種是遠親,這表明每個具有大型Hil家族的物種都是獨立進化出家族規(guī)模的,而不是基因遺傳下來的。
生物學(xué)系助理教授、該研究的共同通訊作者Bin He說,“我們發(fā)現(xiàn)這個基因家族在病原酵母譜系中通過基因復(fù)制而特定地反復(fù)擴大,此外,它們的序列在復(fù)制后迅速進化,可能產(chǎn)生了功能多樣性,使酵母適應(yīng)復(fù)雜的宿主環(huán)境。”
適應(yīng)因素是關(guān)鍵:Hil基因可能編碼蛋白質(zhì),使生物體成為粘合劑。更具體地說,這些蛋白質(zhì)通過其結(jié)構(gòu),幫助酵母細胞粘附在宿主組織和無生命的表面(如導(dǎo)管)上,并將自己縫合在一起,就像環(huán)環(huán)相扣的樂高積木一樣,形成一堵幾乎不可穿透的耐藥墻,稱為生物膜。
這是最好的自然選擇,或者可以說是最邪惡的自然選擇。希爾基因在一些其他酵母物種中要么不存在,要么不活躍,比如面包師酵母,這些酵母實際上對人類有益(假設(shè)人們喜歡面包)。但研究人員發(fā)現(xiàn),在致病的物種中,Hil (Hyr/Iff-like的簡稱)家族非常活躍,并對其粘附性造成嚴重破壞。
“這就是趨同進化,你找到了在環(huán)境利基領(lǐng)域取得成功的方法。”
研究人員對粘附蛋白家族中的蛋白質(zhì)進行了測序,并搜索了所有其他生物——包括植物、動物和細菌王國——以找出是否有其他物種具有類似的蛋白質(zhì)序列。他們只在一個地方發(fā)現(xiàn)了Hil基因家族,即酵母菌類,真菌王國的一部分。
分析揭示了另一個重要的線索:希爾家族出現(xiàn)在沒有近親的物種中,從分類學(xué)上講。例如,Hil?家族在C. auris和另一種致病物種白色念珠菌中存在并活躍。但當研究人員觀察每個物種的親緣關(guān)系更密切時,Hil基因的數(shù)量要么很低,要么根本不存在。
He說,“這是一種平行或獨立的進化,基本上,這些基因達到了相同的最終狀態(tài),不是通過下降,也不是通過遺傳,而是通過獨立進化。它們都走了相似的進化道路。”
這項研究本身起源于愛荷華州的一門研究生級別的生物信息學(xué)課程。2019年秋季,該課程的講師將課程集中在C. auris上,它的5000個基因基因組最近剛剛被測序。一個學(xué)生小組決定調(diào)查C. auris對粘性的偏好。
這是一個明智而富有成效的選擇。
“我們根據(jù)帶有關(guān)鍵字的域選擇蛋白質(zhì),我們認為這些蛋白質(zhì)可能與真菌病原體的粘性有關(guān),并得出了這組粘附素,當時,在我們研究的基因組中報告了兩個小的粘附蛋白家族,所以一旦我們意識到這個(Hil)家族有多大,我們就非常確定我們在這個物種中發(fā)現(xiàn)了一些還沒有被特征化的東西。”
生物系教授Jan Fassler與生物學(xué)副教授Albert Erives在2013年構(gòu)想了這門課程。他說,教師們會選擇文獻中出現(xiàn)過的、具有有趣生物學(xué)屬性的基因組。
“我們選擇了最近測序的基因組,這樣就很少有事先調(diào)查,從而讓學(xué)生們感覺他們(而且他們正在)有新的發(fā)現(xiàn)。”
研究人員接下來想通過實驗來調(diào)查,特別是Hil家族是如何讓C. auris成為粘合劑的。這將推動研究的發(fā)展,超越識別相關(guān)基因的范疇,并可能導(dǎo)致醫(yī)學(xué)進步。
“希望是這樣的:我們已經(jīng)確定了一個基因家族,它可能在發(fā)病機制中發(fā)揮重要作用,并且僅限于這組真菌。如果我們能找到抑制它的方法,這可能是一個藥物靶點,”He說。

